Nell’adulto e soprattutto nell’anziano, l’ipotiroidismo non agisce come causa diretta della scoliosi, ma come fattore di progressione e aggravamento di deformità già presenti (scoliosi degenerativa o idiopatica evoluta). I principali meccanismi coinvolti includono alterazioni del metabolismo osseo, effetti diretti del TSH sul tessuto osseo e alterazioni muscolari e posturali.
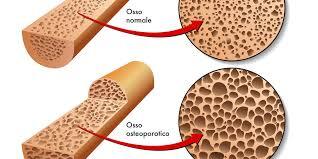
L’ipotiroidismo determina una riduzione del turnover osseo, con un osso strutturalmente più vecchio e meno capace di adattarsi ai carichi meccanici. La qualità ossea può risultare compromessa anche in assenza di osteoporosi evidente alla densitometria ossea (MOC).
Il TSH non rappresenta solo un marcatore di funzione tiroidea, ma esercita effetti diretti sul tessuto osseo attraverso recettori espressi su osteoblasti e osteoclasti. Valori elevati di TSH inibiscono il rimodellamento osseo, favorendo microdanni strutturali vertebrali non sempre rilevabili con la MOC.
L’ipotiroidismo è associato a sarcopenia, riduzione della forza dei muscoli paravertebrali e peggior controllo posturale. Questi fattori contribuiscono ad aumentare le asimmetrie di carico sulla colonna vertebrale, favorendo la progressione della scoliosi.
La severità della scoliosi non si correla necessariamente con la densità minerale ossea. Questo suggerisce che la qualità ossea e la microarchitettura vertebrale siano più rilevanti della quantità di minerale misurata dalla MOC.
L’ipotiroidismo e l’elevazione del TSH possono favorire i crolli vertebrali da fragilità attraverso una ridotta capacità di riparazione delle microfratture, aumento della rigidità ossea e maggiore esposizione a carichi asimmetrici. I crolli, anche subclinici, possono innescare un circolo vizioso di peggioramento della deformità.
Nei pazienti anziani con scoliosi dell’adulto è fondamentale valutare non solo la densità minerale ossea, ma anche la funzione tiroidea, considerando l’ipotiroidismo come fattore di rischio per la progressione deformativa e per i crolli vertebrali.
Nei pazienti con deformità vertebrali dell’adulto, l’ipotiroidismo risulta frequente e si associa a una maggiore severità della scoliosi, espressa da un incremento dell’angolo di Cobb. È quanto emerge da uno studio multicentrico retrospettivo pubblicato su Spine Deformity, che ha analizzato la relazione tra disfunzione tiroidea e scoliosi degenerativa nella popolazione anziana.
Studi precedenti avevano già suggerito una maggiore prevalenza di ipotiroidismo nei pazienti affetti da patologie degenerative della colonna vertebrale; tuttavia, il suo possibile ruolo nella gravità della deformità non era stato chiaramente definito.
Lo studio ha incluso 834 pazienti di età pari o superiore a 60 anni, valutati tra agosto 2015 e novembre 2024, con evidenza radiologica di deformità vertebrale misurata mediante angolo di Cobb. L’età media era di 80 anni; 596 pazienti erano di sesso femminile.
La scoliosi degenerativa dell’adulto era presente nell’80,3% dei casi, mentre il 19,7% presentava una scoliosi idiopatica dell’adolescenza progredita in età adulta. L’angolo di Cobb medio era di 18,3° nel primo gruppo e di 28,4° nel secondo.
Complessivamente, il 33,3% dei pazienti presentava una diagnosi di ipotiroidismo. Nei soggetti con scoliosi degenerativa, la presenza di ipotiroidismo, l’aumento dei livelli di TSH e il sesso femminile risultavano significativamente associati a una maggiore entità dell’angolo di Cobb. Al contrario, non è stata osservata alcuna associazione significativa tra funzione tiroidea e densità minerale ossea.
Questi risultati indicano che l’ipotiroidismo è più prevalente nei pazienti con deformità vertebrali dell’adulto rispetto alla popolazione generale e che il TSH rappresenta un potenziale indicatore di rischio per la progressione della scoliosi degenerativa. La densità minerale ossea, invece, non sembra influenzare direttamente la gravità della deformità.
RIFERIMENTO
Spine Deformity. 2026 Jan 11. doi: 10.1007/s43390-025-01269-8. Online ahead of print.
OSSO E TIROIDE : Azioni e meccanismi biochimico-molecolari degli ormoni tiroidei su osso e osteoporosi
Gli ormoni tiroidei (soprattutto la triiodotironina, T3) regolano in modo diretto e indiretto il rimodellamento osseo. L’effetto finale dipende dall’equilibrio fra formazione (osteoblasti) e riassorbimento (osteoclasti), dal contesto (età, sesso, carico meccanico) e dallo stato tiroideo (eutiroidismo, ipotiroidismo, ipertiroidismo o forme subcliniche).
Gli ormoni tiroidei T4 e T3 entrano nelle cellule ossee tramite trasportatori di membrana; nel microambiente scheletrico, la conversione locale di T4 in T3 (enzimi deiodinasi) contribuisce a modulare l’intensità del segnale tiroideo. La T3 è la forma biologicamente più attiva e rappresenta il ligando principale dei recettori nucleari.
La T3 si lega ai recettori tiroidei (TR), in particolare TRα (TRα1), ampiamente espressi in cellule della linea osteoblastica e nel compartimento cartilagineo/osseogenico. Il complesso T3–TR agisce come fattore di trascrizione e regola l’espressione genica di proteine coinvolte in differenziamento, maturazione e attività delle cellule ossee.
In condizioni di eccesso di ormoni tiroidei, la T3 può accelerare la maturazione osteoblastica e aumentare l’espressione di mediatori che favoriscono l’osteoclastogenesi. Un asse cruciale è il sistema RANKL/OPG:
- RANKL (espresso da osteoblasti/osteociti) stimola la differenziazione degli osteoclasti;
- OPG (osteoprotegerina) è un recettore-esca che sequestra RANKL e ne riduce l’effetto.
L’aumento relativo di RANKL (e/o la riduzione di OPG) sposta il bilancio verso il riassorbimento osseo.
La T3 può stimolare la differenziazione degli osteoclasti anche tramite l’attivazione di programmi trascrizionali pro-osteoclastogenici (es. vie immediate-early come c-Fos) e mediante l’incremento dei segnali provenienti dagli osteoblasti (RANKL). Ne risulta un aumento del riassorbimento e un’accelerazione del ciclo di rimodellamento.
Gli osteociti regolano il rimodellamento integrando segnali meccanici e molecolari. Gli ormoni tiroidei interagiscono con reti di segnalazione (tra cui Wnt) che coordinano formazione e riassorbimento; questo è rilevante perché le deformità vertebrali (es. scoliosi degenerativa) amplificano carichi asimmetrici e microdanno, richiedendo un rimodellamento “di qualità” per mantenere la resistenza vertebrale.
Evidenze sperimentali mostrano l’espressione del recettore del TSH (TSHR) su precursori osteoblastici e osteoclastici, suggerendo un’azione diretta del TSH sul rimodellamento. In particolare, il TSH viene descritto come regolatore negativo del turnover (effetto inibitorio su riassorbimento e, in parte, su formazione), contribuendo a “frenare” il rimodellamento. Ciò rende plausibile che livelli di TSH e stato tiroideo possano influenzare non solo la densità minerale, ma anche la qualità ossea e la suscettibilità a fratture.
- Ipertiroidismo (anche subclinico con TSH soppresso): aumenta il turnover osseo e riduce il tempo del ciclo di rimodellamento; il riassorbimento tende a superare la formazione, con perdita di massa ossea (soprattutto corticale), aumento della porosità e incremento del rischio di fratture.
- Ipotiroidismo: riduce il turnover; la BMD può risultare normale o talora aumentata, ma l’osso può accumulare microdanni e “invecchiare” (minore capacità di riparazione e adattamento), con possibile incremento della fragilità anche quando la MOC non evidenzia osteoporosi marcata.
In presenza di scoliosi dell’adulto, dove i carichi vertebrali sono già disomogenei, questi meccanismi possono facilitare microfratture, crolli vertebrali e progressione deformativa.
Biografia
- Abe E, et al. TSH Is a Negative Regulator of Skeletal Remodeling. Cell. 2003.
- Williams GR, et al. Actions of thyroid hormones in bone (review). Endokrynologia Polska. 2009.
- Ma R, et al. The Influence of Thyroid-Stimulating Hormone and Thyroid Hormones on Bone. 2011.
- Blum MR, et al. Subclinical Thyroid Dysfunction and Hip Fracture and Bone Mineral Density. J Clin Endocrinol Metab. 2015.
- JAMA Network Open. Association Between Subclinical Thyroid Dysfunction and Fracture Risk. 2022.
- Endocrinol Metab (Seoul). Evaluation and Management of Bone Health in Patients with Thyroid Diseases. 2023.
- Spine Deformity. 2026 Jan 11. doi:10.1007/s43390-025-01269-8.