Nella pratica clinica della tiroide, l’esame di riferimento resta l’ecografia bidimensionale (2D) ad alta risoluzione con studio Doppler, integrata quando serve da agoaspirato, elastografia o altre tecniche multiparametriche. Nella letteratura, però, negli ultimi anni è cresciuto l’interesse verso la ricostruzione tridimensionale (3D) dell’organo e dei noduli tiroidei, ottenuta con sonde dedicate o con sistemi “freehand” che ricostruiscono un volume a partire da scansioni 2D. Le principali società scientifiche internazionali continuano tuttavia a considerare la 2D come standard di riferimento; la 3D è vista soprattutto come tecnica promettente, non ancora routinaria.
Il termine “tomosintesi tiroidea 3D” non è oggi uno standard lessicale universale nelle linee guida tiroidee, dove si parla più spesso di 3D ultrasound, volumetric ultrasound, freehand 3D ultrasound o tracked 3D ultrasound. In ambito senologico “tomosintesi” indica una tecnica radiologica a raggi X; nella tiroide, invece, il termine è usato in modo meno uniforme e di solito fa riferimento a ricostruzioni volumetriche ecografiche tridimensionali. Pertanto è più corretto parlare di ecografia tiroidea 3D o tomosintesi ecografica 3D della tiroide.
Per lo studio ecografico della tiroide le società scientifiche raccomandano una sonda lineare ad alta frequenza, in genere nell’ordine di 10–15 MHz, con alcuni documenti che citano valori minimi di 7,5 MHz o preferibilmente 12 MHz per l’elevata risoluzione delle strutture superficiali del collo. Questo vale anche quando si voglia costruire un dataset 3D di buona qualità, perché la base resta comunque l’acquisizione ecografica ad alta frequenza.
Nella pratica, i sistemi 3D descritti in letteratura si dividono in tre gruppi principali:
1. sonde lineari convenzionali 2D con ricostruzione freehand 3D, spesso assistita da sensori giroscopici o di tracking;
2. sonde matrix-array / matrix 3D, capaci di acquisire volumi in modo più diretto;
3. sistemi sperimentali o avanzati con tracking software, segmentazione automatica o intelligenza artificiale. Studi recenti citano, ad esempio, ricostruzioni freehand con guida giroscopica e matrix transducer per volumetria nodulare e supporto alle procedure interventistiche.
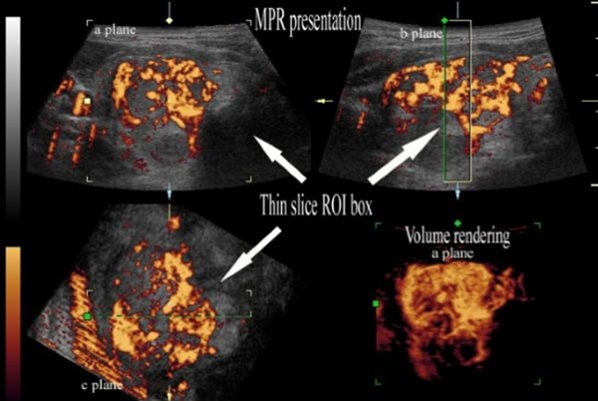
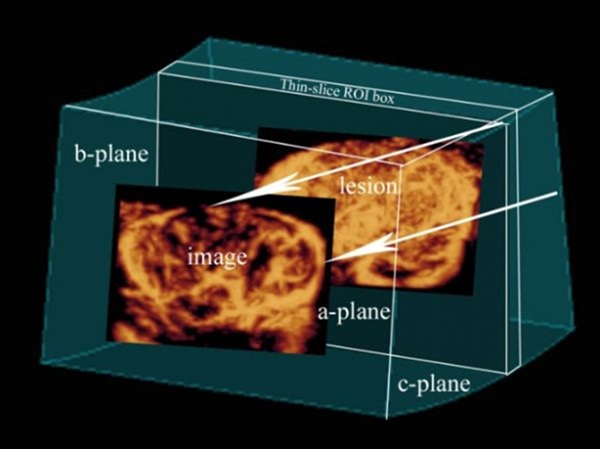
Nell’ecografia 3D tiroidea il clinico acquisisce una sequenza di immagini 2D lungo il decorso del lobo o del nodulo; un software ricostruisce poi un volume tridimensionale visualizzabile nei piani assiale, sagittale e coronale, oltre che come rendering volumetrico. Questo permette di analizzare meglio la morfologia spaziale della lesione, di archiviare l’intero volume e di riesaminare il caso anche in un secondo momento.
La 3D è ritenuta utile soprattutto per quattro motivi.
Primo: migliora la valutazione volumetrica di tiroide e noduli. Diversi studi recenti indicano che la 3D può essere più accurata e riproducibile della 2D per la misura dei volumi, riducendo l’errore legato all’approssimazione ellissoidale e alla variabilità dell’operatore.
Secondo: può migliorare il follow-up nel tempo, perché consente di confrontare interi volumi invece di sole misure lineari. Questo è particolarmente interessante nei noduli benigni sorvegliati, dove piccole variazioni dimensionali possono essere difficili da interpretare con la sola 2D.
Terzo: può aiutare nella pianificazione e nel monitoraggio delle procedure mini-invasive, per esempio agoaspirato o termoablazione, perché una migliore stima del volume e dell’estensione tridimensionale può favorire il targeting e la valutazione del risultato. In studi sperimentali la sonda matrix 3D ha mostrato una stima volumetrica più accurata e la potenziale capacità di facilitare il posizionamento dell’ago e ridurre i tempi procedurali.
Quarto: la 3D è interessante per la ricerca, l’AI e la radiomica, perché fornisce informazioni spaziali più ricche rispetto alla singola immagine 2D. Questo potrebbe in futuro migliorare segmentazione, classificazione e standardizzazione del referto.
Ad oggi la 3D tiroidea non va considerata un esame di primo livello obbligatorio per tutti i pazienti con nodulo tiroideo. Le principali indicazioni ragionevoli sono selettive:
- follow-up di noduli in cui si desideri una volumetria più precisa;
- gozzo o tiroide strutturalmente alterata, quando la misura del volume abbia un impatto clinico;
- valutazione pre- e post-procedura in termoablazione o altre tecniche interventistiche;
- contesti di ricerca o centri con esperienza specifica.
Invece, nella pratica standard del nodulo tiroideo, l’iter resta quello basato su ecografia 2D ad alta risoluzione, classificazione del rischio ecografico con sistemi come ATA, EU-TIRADS, ACR TI-RADS o K-TIRADS, e indicazione all’agoaspirato secondo criteri ecografici e dimensionali. Nessuno di questi principali sistemi di stratificazione richiede oggi la 3D come criterio routinario.
I vantaggi teorici e pratici della 3D sono:
- disponibilità tecnologica non omogenea;
- necessità di software dedicati e training;
- tempi e workflow non sempre compatibili con l’attività ambulatoriale ordinaria;
- evidenza clinica ancora limitata rispetto alla 2D standard;
- mancanza, nelle linee guida maggiori, di raccomandazioni forti a favore dell’uso routinario.
La letteratura internazionale è favorevole ma prudente.
Uno studio del 2012 ha mostrato che, per tutti i lettori, l’interpretazione con immagini 3D era più sensibile e più specifica rispetto alla 2D nella distinzione tra noduli benigni e maligni; questo risultato è interessante, ma non è bastato da solo a cambiare la pratica clinica globale.
Una review del 2011 concludeva che la 3D ultrasound è pratica e riproducibile per la valutazione dei noduli tiroidei e che consente di memorizzare volumi comprendenti l’intera lesione o l’intero organo. Già allora, tuttavia, si sottolineava che i vantaggi principali erano soprattutto morfologici e volumetrici, più che di sostituzione dello standard 2D.
Una review del 2015 sulle innovazioni nell’ecografia tiroidea considerava il possibile ruolo della 3D thyroid ultrasound tra i futuri sviluppi tecnici, quindi come evoluzione promettente ma non ancora parte dello standard consolidato.
Negli studi più recenti il filone più convincente riguarda la volumetria. Un lavoro del 2021 con matrix 3D ultrasound ha riportato che il trasduttore matrix 3D stima i volumi in modo più accurato e può facilitare il corretto posizionamento dell’ago riducendo il tempo procedurale. Studi del 2022–2025 su sistemi tracked/freehand e segmentazione assistita da AI riportano una migliore accuratezza e riproducibilità della 3D rispetto alla 2D, soprattutto per la misura dei volumi tiroidei.
Nel complesso, quindi, la letteratura suggerisce che la 3D abbia potenziale reale, soprattutto in volumetria, follow-up e interventistica, ma che le evidenze siano ancora insufficienti per sostituire la 2D nella valutazione standard del nodulo tiroideo.
Cosa dicono le società scientifiche
American Thyroid Association (ATA)
Le linee guida ATA per i noduli tiroidei e il carcinoma differenziato considerano l’ecografia l’esame chiave per definire anatomia, caratteristiche del nodulo e rischio, ma non introducono la 3D come passaggio obbligatorio o standardizzato nel percorso diagnostico. L’ATA mantiene quindi una posizione centrata sulla ecografia convenzionale di alta qualità.
European Thyroid Association (ETA)
Le linee guida ETA per i noduli tiroidei e il carcinoma differenziato considerano l’ecografia l’esame chiave per definire anatomia, caratteristiche del nodulo e rischio, ma non introducono la 3D come passaggio obbligatorio o standardizzato nel percorso diagnostico. L’ETA mantiene quindi una posizione centrata sulla ecografia convenzionale di alta qualità.
American College of Radiology (ACR)
L’ACR TI-RADS usa i classici criteri ecografici del nodulo — composizione, ecogenicità, margini, forma ed echi puntiformi — per guidare follow-up e biopsia. La piattaforma ACR e il TI-RADS non richiedono una valutazione 3D routinaria.
ACR–AIUM–SPR–SRU Practice Parameter
Il practice parameter congiunto per l’ecografia tiroidea definisce tecnica, documentazione ed esecuzione dell’esame e specifica che le dimensioni di ciascun lobo vadano registrate in tre dimensioni lineari (antero-posteriore, trasversale e longitudinale). Questo però non equivale a raccomandare la ricostruzione volumetrica 3D; indica piuttosto lo standard di refertazione della 2D convenzionale.
Korean Society of Thyroid Radiology (KSThR)
Anche i documenti coreani più recenti puntano su ecografia ad alta risoluzione con sonda lineare 10–15 MHz, refertazione standardizzata e sistemi di stratificazione del rischio. La 3D non è descritta come requisito di routine.
Conclusioni
La tomosintesi/ecografia tiroidea 3D è una metodica interessante e in evoluzione. Le sonde usate sono in primo luogo lineari ad alta frequenza, talora integrate con sistemi di tracking, giroscopi o trasduttori matrix 3D. La tecnica è utile soprattutto per volumetria più precisa, follow-up dei noduli, supporto alle procedure interventistiche e applicazioni di ricerca/AI.
Tuttavia, allo stato attuale, la letteratura internazionale la considera una tecnologia promettente ma non ancora standard. Le principali società scientifiche — ATA, ETA, ACR, AIUM e KSThR — continuano a fondare la pratica clinica sulla ecografia 2D ad alta risoluzione, mentre la 3D resta indicata soprattutto in casi selezionati e in centri con competenze dedicate.
Biografia essenziale
1. Haugen BR et al. 2015 American Thyroid Association Management Guidelines. Thyroid.2. Durante C et al. 2023 European Thyroid Association Clinical Practice Guidelines for thyroid nodules. Eur Thyroid J.
3. Tessler FN et al. ACR TI-RADS / ACR thyroid resources.
4. ACR–AIUM–SPR–SRU. Practice Parameter for Diagnostic Ultrasound of the Thyroid and Extracranial Head and Neck.
5. Lee MK et al. Standardized Imaging and Reporting for Thyroid Ultrasound. Korean J Radiol. 2023.
6. Slapa RZ et al. Advantages and disadvantages of 3D ultrasound of thyroid lesions. 2011.
7. McQueen AS et al. Thyroid nodule ultrasound: technical advances and future trends. 2015.
8. Jang M et al. Differentiating benign from malignant thyroid nodules. 2012.
9. Boers T et al. Ultrasound imaging in thyroid nodule diagnosis, therapy, and follow-up: current status and future trends. 2023.
10. Cheng A et al. Use of 3D ultrasound to characterise temporal changes in thyroid nodules. 2023.
11. Boers T et al. Matrix 3D ultrasound-assisted thyroid nodule volume estimation. 2021.
12. Seifert P et al. Optimization of thyroid volume determination by stitched 3D ultrasound datasets. 2023.
13. Krönke M et al. Tracked 3D ultrasound and deep neural network-based thyroid segmentation. 2022.
14. Rask KB et al. AI-assisted freehand 3D ultrasound for thyroid volume measurement. 2025.