Il microbiota regola il sistema immunitario; probiotici e prebiotici possono aiutare a prevenire e migliorare il decorso delle sindromi autoimmuni compresa la Tiroidite di Hashimoto e il Morbo di Basedow.
Il microbiota umano (flora intestinale) è l'insieme di microorganismi simbiontici che convivono con l'organismo umano senza danneggiarlo. Nelluomo ci sono tra 500 e 10.000.000 specie differenti di microorganismi, i più numerosi dei quali sono batteri, ma anche in misura inferiore miceti e virus. |
 |
Il batterio intestinale più conosciuto nell'Uomo è l'Escherichia coli.
Il microbiota umano si sviluppa nel corso dei primi giorni di vita e sopravvive, salvo in caso di malattie, sorprendentemente a lungo.
Ogni individuo possiede il suo proprio microbiota, i ricercatori dell'INRA hanno messo in evidenza l'esistenza di un piccolo numero di specie condivise da tutti che costituirebbero il nucleo filogenetico del microbiota intestinale umano.
Il numero di geni totale del microbiota (microbioma) è stimato essere 100 volte il numero di geni del genoma umano.
Un'importante funzione del microbiota umano è la disgregazione delle sostanze che il nostro sistema non è in grado di smantellare, come le cartilagini e le molecole di cellulosa. Un'altra funzione importante è la sintesi di sostanze indispensabili, ad esempio la vitamina K, che svolge un ruolo essenziale nella coagulazione del sangue. In rari casi, può capitare che il microbiota intestinale del neonato non sia ancora in grado di produrre la vitamina K e quindi, in via precauzionale, ogni neonato ne riceve un'iniezione intramuscolare.
Pertanto, il microbiota dovrebbe essere considerato come un organo vero e proprio: il microbiota può essere considerato come un organo metabolico “adattato” alla nostra fisiologia che svolge funzioni che non siamo in grado di svolgere altrimenti. Tali funzioni includono la capacità di assimilare componenti altrimenti indigeribili della nostra dieta, come i polisaccaridi vegetali.
Alla nascita il tratto digerente dei neonati è completamente sterile e viene colonizzato immediatamente, a partire dal parto, dai microorganismi con cui viene in contatto provenienti dal tratto riproduttivo e fecale della madre; successivamente i batteri provengono dall'allattamento, dall'ambiente, e infine dai cibi che nel tempo ingerirà.
I tratti digerenti di neonati partoriti con cesareo vengono colonizzati inizialmente da batteri presenti nell'ambiente, non venendo in contatto con quelli della madre, e similmente i neonati non allattati naturalmente saranno maggiormente colonizzati da batteri ambientali piuttosto che di derivazione umana.
La differenza principale tra questi iter è che la stabilizzazione (100 miliardi di batteri per grammo di feci) del microbiota dei neonati naturali avviene dopo un mese e viene composto maggiormente da Bifidobacteria, mentre nelle altre circostanze non si stabilizza per almeno 6 mesi e viene composto prevalentemente da Enterobacteriaceae ed Enterococci.
“Viene da chiedersi se questa esplosione di malattie autoimmuni (in primis celiachia e tiroiditi autoimmuni, psoriasi e asma), dell’epoca moderna, derivi proprio dal fatto che i parti non vengano più o quasi mai eseguiti per via naturale ma con taglio cesareo e che non sempre viene perseguito l’allattamento al seno materno !!...”
Venendo all’argomento oggetto della presente trattazione, il microbiota ha un ruolo cruciale nelle sindromi autoimmuni sistemiche come artrite reumatoide, lupus eritematoso, sindrome di Sjogren, morbo di Chron e anche nelle tiroiditi autoimmuni sia ipo (Tiroidite di Hashimoto) che iperfunzionanti (M. di Basedow).
Nel mese di ottobre e novembre 2016, due lavori pubblicati sulla rivista Oral Disease, hanno dimostrato che la disbiosi del microbiota e l’aumento di batteri specifici possono produrre metaboliti tossici ad azione infiammatoria della mucosa e di incremento della permeabilità intestinale. Di conseguenza, la produzione locale di linfociti e di citochine proinfiammatorie si riversa nel circolo ematico e aumenta il rischio di flogosi multisistemica a carico di diversi organi e apparati: articolazioni, ghiandole salivari, tiroide etc.
La conferma che il microbiota regola i componenti del sistema immunitario, apre la possibilità a nuove strategie terapeutiche per trattare e prevenire le malattie autoimmuni.
Probiotici e prebiotici agiscono sul ripristino e il mantenimento del microbiota in eubiosi (equilibrio).
È quanto osservato dai ricercatori del Department of Oral and Maxillofacial Surgery, University of Groningen, Netherlands e dal Department of Oral Pathology and Medicine, University of Athens, Greece.
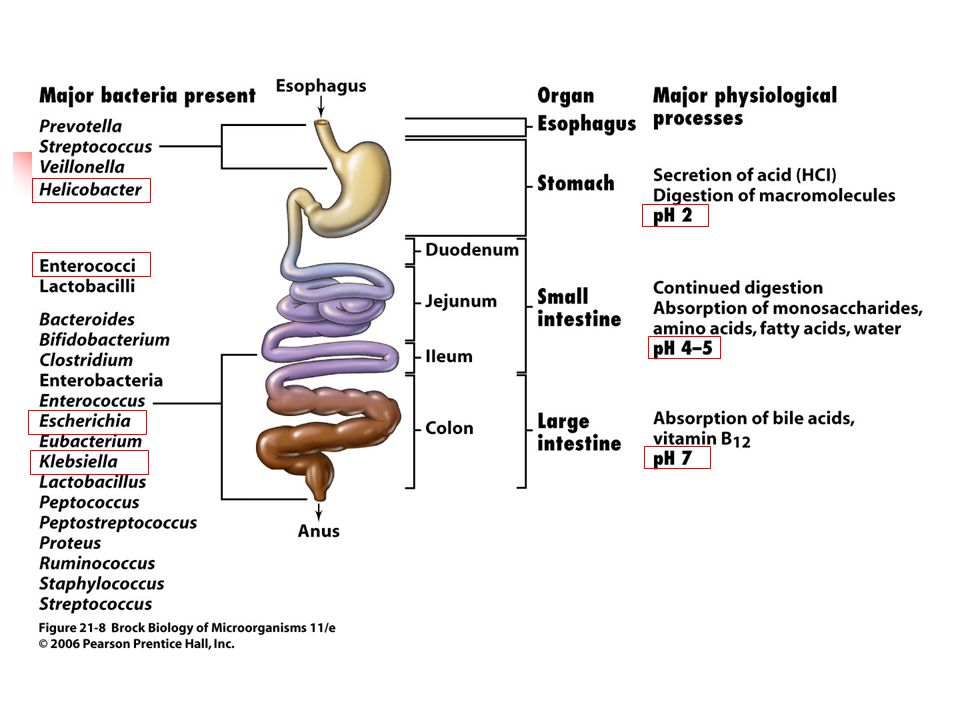
Il microbiota umano si trova sulla pelle, sulle membrane delle mucose e nell’intestino, in particolare il colon.
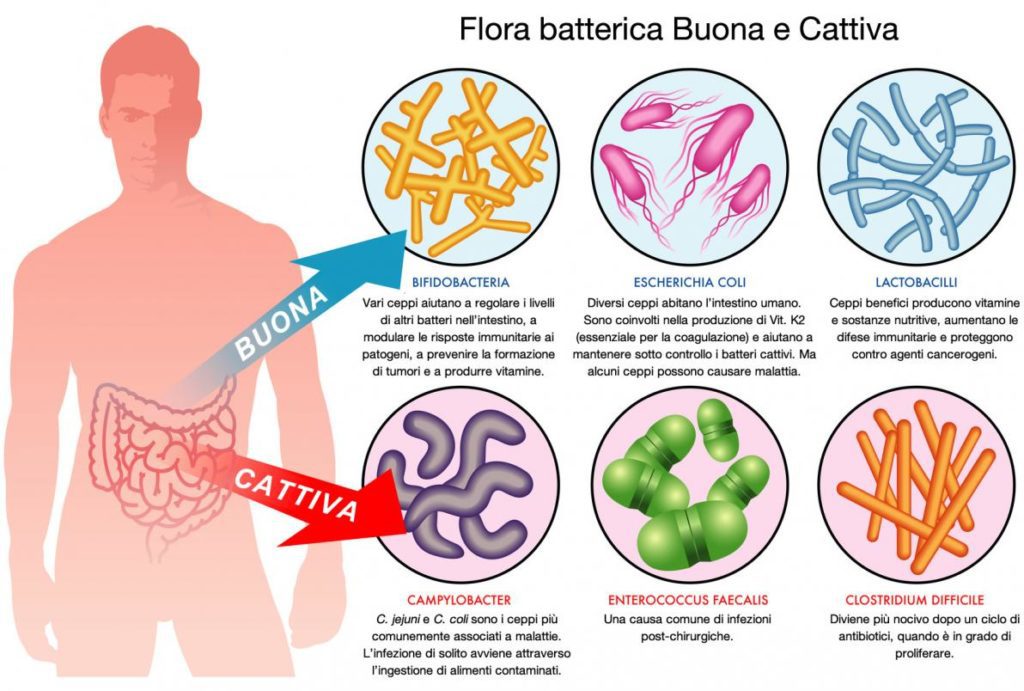
Grazie al sequenziamento del DNA e agli studi sul microbioma umano (geni della flora batterica), abbiamo un elenco quasi completo delle comunità microbiche presenti.
Il microbiota ha un ruolo importante nella sintesi di vitamine e influenza l’immunità sistemica, ossia la formazione di immunoglobuline IgA (difensori della superficie del nostro organismo da tossine e batteri patogeni), e di cellule T regolatrici, Treg (ad azione immunosoppressiva).
Nella disbiosi intestinale, causata da una dieta sbilanciata, da antibiotici, da stress psicologico e fisico, avvengono alterazioni nel metabolismo batterico, così come la sovracrescita di microrganismi potenzialmente patogeni; le cellule T infiammatorie, tipo Th1 e Th17 aumentano, e le cellule Treg (immunosoppressorie) diminuiscono. La barriera intestinale danneggiata diventa permeabile e permette a cellule e molecole pro-infiammatorie di diffondersi in vari distretti.
È stato riscontrato che nelle malattie autoimmuni, il sistema immunitario è squilibrato verso uno stato infiammatorio cronico; l’aumento della permeabilità intestinale incrementa l’esposizione agli antigeni e il rischio di produzione degli autoanticorpi. Pertanto, le alterazioni della flora intestinale sono state associate allo sviluppo di malattie infiammatorie e autoimmuni.
Nell’artrite reumatoide, nel lupus eritematoso e nella sindrome di Sjogren la disbiosi intestinale si manifesta con una carenza di Bifidobatteri e un aumento di Prevotella; nel morbo di Crohn e la colite ulcerosa, sono stati individuati livelli elevati di Escherichia coli. Vengono utilizzati metodi non invasivi per ripristinare l’eubiosi intestinale come l’assunzione di probiotici Lactobacillus Rhamnosus o Lactobacillus Reuteri, per migliorare la funzione della barriera intestinale e prebiotici (fibre solubili), per stimolare la crescita del microbiota. Tutto associato ad una dieta congrua e salutare a base di frutta, legumi e verdure.
In commercio esistono prodotti con ceppi specifici di fermenti lattici specifici ad azione immuno-riequilibrante su substrato di polisaccaridi microglobulari tipo 1-3 beta-glucano ad effetto attivante macrofagico e con vit C che contribuisce al normale funzionamento del sistema immunitario.
I Beta-Glucani sono polisaccaridi strutturali di piante, lieviti e funghi, con peso molecolare tra 20000 e 5000000, costituiti da unità glicosidiche non ramificate unite da legami chimici 1-4 Beta con intercalati legami 1-3-Beta il cui rapporto varia con l’età dell’organismo di cui fanno parte.
I Beta-Glucani sono presenti principalmente nell’endosperma dei cereali, in particolare orzo e avena, nelle pareti cellulari del lievito saccharomyces e nelle ife fungine enzimaticamente attive di alcuni funghi su composti vegetali di varia natura.
I Beta-Glucani 1-4 sono estratti da orzo e avena, sono idrosolubili e sono conosciuti per le proprietà ipocolesterolemizzanti.
I Beta-Glucani 1-3 sono di derivazione da funghi medicinali e dai loro composti di coltura (crusca di orzo e di riso inoculata con ife fungine) e hanno applicazione in oncologia.
I Beta-Glucani 1-3, derivanti dalla parete cellulare del lievito saccharomyces, hanno invece azione immunostimolante aspecifica.
I Beta Glucani, se estratti in forma pura e certificata, stimolano i macrofagi, che sono tra le più importanti cellule del nostro sistema immunitario, che vengono appunto attivati in forza di recettori specifici.
Tale sensibilizzazione macrofagica è il primum movens della cascata immunitaria che porta all’attivazione delle linee cellulari linfoidi e mieloidi.
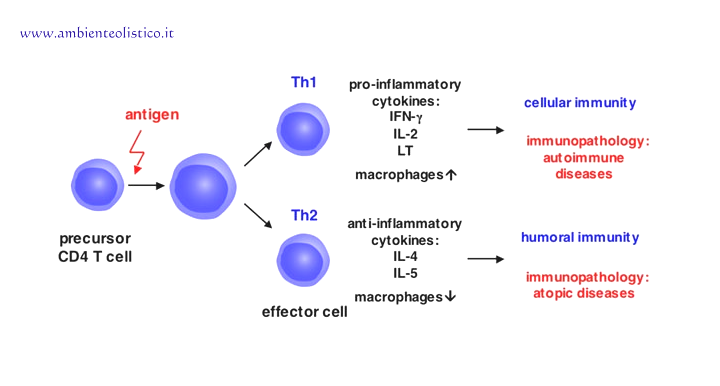
Il macrofago infatti determina l’immissione in circolo, da parte dei linfociti,di citochine (sostanze di natura proteica come le interleuchine, interferone, fattori di necrosi cellulare etc.), ossia di messaggeri chimici che determinano l’assetto e l’equilibrio delle risposte immunitarie sia Th1 (cellulo mediata) che Th2 (umorale).
Tale equilibrio deve essere mantenuto e perfettamente regolato per evitare e prevenire reazioni immunitarie abnormi.
La vitamina C svolge azione sinergica sui macrofagi e spesso la si ritrova nei migliori prodotti pre/probiotici in commercio.
La modulazione dell’immunità è garantita da meccanismi complessi che si articolano, come già detto, in due modalità: la risposta di tipo Th1, ossia cellulo mediata, tipica della tiroidite di Hashimoto, e quella Th2, ossia di tipo umorale/anticorpale, tipica del m. di Basedow.
Tali modalità di risposta devono essere in equilibrio e mantenute al fine di garantire l’ottimale funzionamento del sistema immunitario. Ciò avviene tramite la produzione di citochine (sostanze prioteiche) come l’interferone gamma e l’interleuchina 10 (IL10).
Diversi sono gli studi che dimostrano che ceppi specifici di Lactobacillus casei e il Bifidobacterium lactis sono particolarmente efficaci nella modulazione dell’IL10 e dell’IFN gamma, come dimostrato tramite dei test effettuati attraverso l’utilizzo delle PBMC (peripheral blood mononuclear cells) che dimostrano la capacità in vitro dei batteri prima citati di stimolare la produzione di citochine.
La supplementazione alimentare di Lactobacillus casei e Bifidobacterium lactis è utile per l’equilibrio della flora intestinale con effetti benefici sul sistema immunitario, e soprattutto contro le infezioni, le infiammazioni, le allergie e le manifestazioni autoimmunitarie. Anche i Beta glucani, in associazione al Lactobacillus casei e Bifidobacterium lactis (CITOGENEX cp, composto simbiontico contenente sia prebiotici che probiotici, ma anche Floravis cp, Swisse probiotic max e Swisse prebiotic ultra, Immunoguardians, Probio forte etc. etc.) hanno dimostrato ottimi risultati sul sistema immunitario con soppressione delle citochine infiammatorie IFN-gamma, IL6 e del VGF (fattore di crescita vascolare endoteliale), inibizione dell’aggregazione infiammatoria e promuovendo la cicatrizzazione di ferite.
Inoltre sembra che riducano anche la perdita di collagene nell’invecchiamento della pelle con rallentamento dell’invecchiamento cutaneo con effetto rivitalizzante.
Il Lactobacillus casei, per esempio, è efficace nel mantenimento della barriera cutanea con efficacia nelle dermatiti atopiche, psoriasi etc.
Il Lactobacillus casei, insieme ad altri probiotici come il Lactobacillus acidophilus e il Bifidobacterium lactis, è stato studiato per la sua funzione di protezione e miglioramento del sistema immunitario e per l’efficacia contro i disturbi autoimmuni: artrite reumatoide, tiroidite di Hashimoto, psoriasi, diabete.
Recentemente, inoltre, si è visto che l'esposizione a un componente cellulare di genere specifico di batteri potrebbe partecipare all’insorgenza e allo sviluppo di disfunzione tiroidea.
Questo componente è il lipopolisaccaride (LPS) presente nella membrana esterna dei batteri Gram-negativi, un composto tossico detto anche endotossina.
L'endotossina direttamente e indirettamente sarebbe in grado di inibire due importanti enzimi che convertono il T4 in T3, e questo a livello del sistema nervoso centrale potrebbe causare la diminuzione del rilascio di TRH e TSH.
Anche nell’ipertiroidismo, lavori del 2014, hanno dimostrato la prevalenza di una flora batterica di enterococchi con carenza di bifidobatteri e lactobacilli.
Ed ancora, una particolare composizione del microbioma sembra facilitare il “riciclo” delle iodotironine: un simile meccanismo è stato già dimostrato per gli ormoni steroidei, per gli acidi biliari e per le vitamine.
Pertanto l’assunzione di prodotti simbiontici (associazione di prebiotici come i beta-glucani e fruttooligosaccaridi e di probiotici mirati) rappresenta un’arma in più, scevra di effetti collaterali, complementare e di supporto ad altri trattamenti farmacologici, verso tutte le patologie autoimmuni ed anche tiroidee.
BIOGRAFIA
- M, Gabrych A, Witkowski JM. Microbiome impact on metabolism and function of sex, thyroid, growth and parathyroid hormones. Acta Biochim Pol. 2016;63(2):189-201.
- Virili C, Centanni M. The role of microbiota in thyroid hormone metabolism and enterohepatic recycling. Mol Cell Endocrinol. 2017 Dec 15;458:39-43. doi: 0.1016/j.mce.2017.01.053. Epub 2017 Feb 4.
- J.M. Pizano(2017) Probiotics and Disease: a comprehensive summary- part 7, Immune Disorders, Integrative medicine, Vol 16, no 5.
- M-S. Kim (2015) Improvement of atopic dermatitis-like skin lesions by IL4 inhibition of P14 protein isolated from lactobacillus casei in NC/Nga mice, Applied Microbiology anf Biotechnology Vol 99(17) pp 7089-2099
- Fengmei Z,Bin D et al(2016 A critical review on production and industrial application of betaglucans, Food Hydrocolloids (2016) 275-288
- Guarner F, Malagelada JR (February 2003). "Gut flora in health and disease". Lancet 361 (9356): 512–9. doi:10.1016/S0140-6736(03)12489-0.PMID 12583961
- Fecal Microflora in Healthy Infants Born by Different Methods of Delivery: Permanent Changes in Intestinal Flora After Cesarean Delivery Grölund, Minna-Maija*†; Lehtonen, Olli-Pekka†; Eerola, Erkki‡; Kero, Pentti*Journal of Pediatric Gastroenterology & Nutrition: January 1999 - Volume 28 - Issue 1 - pp 19-25
- Coppa GV, Bruni S, Morelli L, Soldi S, Gabrielli O (July 2004). "The first prebiotics in humans: human milk oligosaccharides". J. Clin. Gastroenterol. 38 (6 Suppl): S80–3.doi:10.1097/01.mcg.0000128926.14285.25. PMID 15220665 Ital J Pediatric 2010 Mar 10;36:24: Autors Rovelli-Vigone et al
- TORNA SU -